II L’action de la lumière sur le Pastis L'été
II L’action de la lumière sur le Pastis
L'été s'achève et le pastis aura coulé à flots. En apparence, le soleil ardent est l'acolyte idéal du "petit jaune" pris en terrasse. En réalité, il est son pire ennemi. C'est ce que nous allons vous démontrer.
a) Absorption de photons :
La lumière possède des propriétés caractéristiques des particules (on peut compter les photons), mais possède aussi des caractéristiques d'ondes électromagnétiques (longueur d'onde, fréquence).
La fréquence est le nombre de fois qu'un phénomène périodique se reproduit pendant une durée déterminée
D'ailleurs, la lumière visible n'est rien d'autre qu’une onde radio qui a une énergie telle qu'elle est "détectée" par nos yeux. Une onde radio est utilisée pour transmettre des signaux de télévision, téléphone... Pour la capter, rien de plus simple, on utilise une antenne. La longueur des antennes dépend de la longueur d'onde donc de la fréquence des signaux qu'on souhaite capter : des grandes antennes pour les ondes radio (qui ont une grande longueur d'onde donc une faible fréquence), et des plus petites antennes pour les téléphones portables (qui utilisent des ondes plus courtes donc des fréquences plus grandes). Il se trouve que les dimensions des molécules (quelques nanomètres) sont de la bonne taille pour « interagir » avec les ondes de grandes énergies (donc grandes fréquences, donc longueurs d'onde très courtes), comme la lumière visible. Les molécules ont toutes des dimensions différentes ce qui fait que chaque molécule absorbe une onde qui lui est propre.
Le nuage électronique d'une molécule (composé d'électrons) agit, en quelque sorte, comme une "antenne" et capte les ondes dont la fréquence est adaptée. La molécule de trans-anéthol, petite, absorbe donc la lumière ultraviolette qui a une longueur d’onde de 380 à 10 nanomètres. La lumière absorbée fournit suffisamment d'énergie pour changer la molécule.
b) Isomérisation trans-cis :
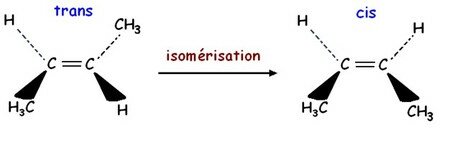
L'énergie apportée par la lumière va permettre l'isomérisation du trans au cis anéthol. La molécule de trans-anéthol modifie sa structure en gardant la même formule brute (nombre et nature des atomes qui la composent). En effet, il n’y a que la disposition de ces atomes qui changent. Ce phénomène s’appelle l’isomérisation. Ceci semble anodin, cependant cela va quand même changer l’odeur de la molécule.
La représentation de Cram, ici, met bien en évidence la géométrie différente dans l’espace de ces deux molécules dû à l’isomérisation
c) Changement d'odeur
L'étude des relations structure/odeur montre que, dans de nombreuses séries, les molécules de structure similaire ont des odeurs voisines, bien que distinguables. Cependant, cette observation n'est pas générale et on connaît de nombreux cas pour lesquels de petites modifications structurales peuvent entraîner des perceptions olfactives totalement différentes comme c'est le cas pour le trans et le cis anéthol.
Les molécules odorantes ne présentent pas de charge électrique globale, elles peuvent pour autant présenter des charges localisées, parfois importantes, qui entraînent la présence de dipôles dans la molécule. Les protéines des récepteurs présentant aussi des dipôles électriques, nous pouvons supposer qu’il y a des interactions entre ces dipôles.
A une odeur correspond un récepteur dont les particularités du site d'interaction peuvent être déduites de l'examen des caractéristiques structurales communes des molécules qui possèdent cette odeur.
Les récepteurs moléculaires portés par les cellules olfactives sont des protéines ressemblant à l’opsine. Les protéines sont particulièrement riches en groupement chimiques CONH, COOH et NH2. Il y a des interactions électriques entres les différents groupements des molécules qui présentent des dipôles électriques et des récepteurs qui présentent eux aussi des dipôles. Ces interactions sont appelées liaisons hydrogènes.
La reconnaissance des molécules par les récepteurs se fait par l’intermédiaire de ces liaisons, qui sont très sensibles à la relation géométrique entre les éléments liés.
Représentation (formule topologique) des molécules de trans et de cis anéthol
N’ayant pas les mêmes liaisons, les récepteurs ne sont alors pas les mêmes donc l’odeur est différente. La molécule ne se fixe pas sur les mêmes récepteurs.
d) Quand le pastis est dilué :
Lorsqu'une molécule de trans-anéthol, responsable du goût anisé, absorbe un photon de lumière, elle se transforme en cis-anéthol, qui a mauvais goût comme nous l’avons démontré précédemment. Or, ce processus est largement ralenti lorsque le trans-anéthol est émulsionné dans un mélange d'eau et d'éthanol. Sous cette forme, les molécules de trans-anéthol sont en effet agrégées et ne cessent de s'entrechoquer : l'énergie acquise à partir de la lumière, qui pourrait les pousser à se transformer en cis-anéthol, est dissipée lors des collisions.
Le trans-anéthol n'aime pas l'eau : il se dissout dans les mélanges eau-éthanol jusqu'à environ 60% d'eau (c'est ce qu'on achète en bouteille). L’eau et l’éthanol sont miscibles en toutes proportions. L’anéthol dans notre cas, totalement soluble dans l’éthanol et pratiquement insoluble dans l’eau. L’éthanol joue un rôle en augmentant la solubilité de l’anéthol : ce dernier est soluble dans des mélanges contenant plus de 40% éthanol. Quand la proportion d’éthanol décroit (lors de la dilution du pastis dans l’eau) le trans-anéthol se sépare et donne lieu à une émulsion. Le trans anéthol, contenu au sein de ces nano-gouttelettes (de quelques dizaines de nanomètres de diamètre) formées suite à cette réaction est moins sensible aux effets (néfastes) de la lumière. A partir du moment où ces agrégats (nano-gouttelettes) de trans-anéthol sont suffisamment nombreux (ce qui arrive lorsque la teneur en eau dépasse 60%) ils s’entrechoquent, dissipant ainsi l’énergie des photons accumulés sans pouvoir subir ainsi d’isomérisation. Cette réaction, qui est responsable de la variation de l’arôme, est inhibée.





/https%3A%2F%2Fassets.over-blog.com%2Ft%2Fcedistic%2Fcamera.png)
/https%3A%2F%2Fstorage.canalblog.com%2F39%2F53%2F425696%2F22441272_p.jpg)
/https%3A%2F%2Fstorage.canalblog.com%2F03%2F34%2F425696%2F22473326_o.jpg)